《化学》电子教案
课题 | 第五章 烃和烃的衍生物 第二节 烃(一) |
教学目标 | 1. 了解甲烷的物理性质和用途;理解甲烷的氧化反应和取代反应 2. 了解烷烃、同系物和烃基的概念 3. 了解简单有机化合物的空间结构、同分异构现象和同分异构体 4. 掌握烷烃的系统命名法 5. 了解乙烯的物理性质和用途,以及烯烃的组成、结构特点和性质;理解乙烯的氧化反应、加成反应和聚合反应 6.了解乙炔的物理性质和用途,以及炔烃的组成、结构特点和性质;理解乙炔的氧化反应 |
教学重点 | 甲烷、乙烯、乙炔的性质和用途 |
教学难点 | 烷烃、烯烃、炔烃的系统命名法,取代反应 |
课时安排 | 3学时 |
教学方法 | 对比-联想结合法,启发式教学与讲练结合法 |
教学手段 | 多媒体辅助,课堂实验 |
教学用具 | 投影仪,化学实验仪器 |
 
【教学进程】
导入
烃是有机化合物中最基本的一大类物质,是有机化合物的母体,其他有机化合物都可以看作是由烃衍生而来的。
讲述
最简单的有机化合物,仅由碳和氢两种元素组成,又叫做碳氢化合物,简称为烃。
板书
烃——仅含有碳和氢两种元素的有机化合物叫烃。
讲述
根据烃分子结构中碳架的不同形式,可把烃分为两大类:链烃和环烃。链烃和环烃根据碳架中所含不同的价键,又可分为不同类别。
烃的简要分类如下:
板书:

CnH2n+2(n≥1)
 
CnH2n(n≥2)
CnH2n-2(n≥2)
CnH2n(n≥3)
CnH2n-6(n≥6)
 
 
 
 
 
讲解
烷烃属于链烃,而甲烷是烷烃中分子组成最简单的物质。
板书
一、甲烷 烷烃
讲述
甲烷俗称沼气、坑气,是池沼底部和煤矿坑道所产生气体的主要成分。此外,有些地方的地下深处蕴藏着大量的天然气,它的主要成分也是甲烷,按体积计,含量一般为80%~90%。这些甲烷都是在隔绝空气的情况下,由植物残体经过某些微生物发酵作用而生成的。
讲述
甲烷分子是由1个碳原子与4个氢原子以共价单键形成的,其分子式为CH4。
板书
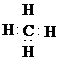
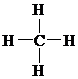
1.甲烷分子的组成与结构。
甲烷的结构:分子式 CH4,电子式 ,结构式 。
 
讲解
科学研究证明,甲烷分子里的碳、氢原子不在同一平面上,而是形成了一个正四面体的立体结构。碳原子位于正四面体的中心,而4个氢原子分别位于正四面体的四个顶点上。碳原子和4个氢原子形成的4个共价键之间的夹角彼此相等,都是109°28′。
演示
甲烷分子的比例模型,让同学们观察,如果配合上投影,播放立体全方位的组成演示效果会更好。
板书
空间结构:正四面体。
过渡
结构决定性质,先了解甲烷的结构,再来学习甲烷的性质。
板书
2. 甲烷的性质。
提问
甲烷有什么样的物理性质?
引导
让学生带着问题读课本,找出问题答案。
指点
甲烷是无色、无臭、无毒的气体,极难溶于水,可溶于煤油、汽油。
讲解
正是由于甲烷分子中碳原子的4个价键都被氢原子所饱和,形成比较牢固的化学键,因此它的化学性质比较稳定。在一般情况下,不跟强酸、强碱、强氧化剂反应。但较纯净的甲烷可在空气中安静燃烧,生成二氧化碳和水,同时放出大量的热。
点燃
板书![]()
(1)氧化反应:CH4+2O2 CO2↑+2H2O。
强调
必须注意,含甲烷5%~15%的空气、甲烷的混合气体,遇火花会立刻发生爆炸。所以,在点燃甲烷前,必须像检验氢气的纯度那样去检验甲烷的纯度。
甲烷跟强氧化剂高锰酸钾也不起反应,不能使高锰酸钾溶液褪色。
引导
甲烷不仅仅和氧气发生反应,在光照的条件下也能和氯气发生反应。
强调
注意:装有甲烷和氯气混合气体的容器不要放在日光直射的地方,否则会引起爆炸。
讲解
甲烷和氯气混合气体的黄绿色逐渐变浅,直至消失,并在容器壁上有油状液滴形成。这说明甲烷与氯气发生了化学反应,反应中首先是甲烷的一个氢原子被一个氯原子所替代,生成一氯甲烷和氯化氢,反应式如下:
光
板书![]()
CH4 + Cl2 CH3Cl + HCl
一氯甲烷
讲解
反应并不停留在这一步,生成的一氯甲烷能继续跟氯气反应,依次生成二氯甲烷、三氯甲烷(氯仿)、四氯甲烷(四氯化碳),反应式如下:
光
板书光
CH3Cl + Cl2 CH2Cl2 + HCl
光
CH2Cl2 + Cl2 CHCl3 + HCl
![]()
CHCl3 + Cl2 CCl4 + HCl
讲解
不难发现甲烷分子中的氢原子是逐步被氯原子所代替的。像这样,有机物分子里的某些原子或基团被其他原子或基团所代替的反应叫做取代反应。
板书
(2)取代反应——有机物分子里的某些原子或基团被其他原子或基团所代替的反应叫做取代反应。
讲述
一氯甲烷等4种取代产物都是甲烷的氯代物。它们都不溶于水。在常温下,一氯甲烷是气体,其他3种都是液体。三氯甲烷和四氯甲烷是工业上重要的溶剂。四氯甲烷还是一种效率较高的灭火剂。
阅读
指导学生阅读课本,结合生活实例说出甲烷的用途。
板书
3. 甲烷的用途——燃料、工业原料。
过渡
除甲烷外,还有一系列结构和性质与它很相似的烃,如乙烷、丙烷、丁烷等。
投影
名称 结构式 结构简式
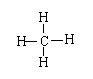
甲烷 CH4
 
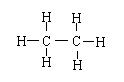
乙烷 CH3CH3
 
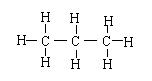
丙烷 CH3CH2CH3
 
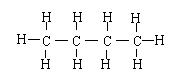
丁烷 CH3CH2CH2CH3
 
引导
在这些烃的分子结构中,碳原子之间以碳碳单键结合成链状,碳原子剩余的价键全部跟氢原子以单键结合,这样的结合使每个碳原子的化合价都达到“和”。
板书
(二)烷烃
1.烷烃的概念。
板书
只有碳碳单键和碳氢键的链烃叫做饱和链烃,也称烷烃。
讲述
烷烃的结构特点是:碳原子之间只存在单键,并且结合成链。
通过比较甲烷、乙烷、丙烷和丁烷的分子结构可以看出,每一个烃都比它前面的烃增加了一个CH2基团。这说明,烷烃分子里碳原子和氢原子的数目之间存在着一定的关系。如果把碳原子数定为n,氢原子数必然等于2n+2,所以,烷烃的分子式可用通式CnH2n+2来表示。
板书
把结构相似,在分子组成上相差一个或若干个CH2基团,并具有同一通式的一系列化合物互称为同系物。烃分子失去一个氢原子后所剩余的基团叫做烃基。
讲解
如果失去氢原子的烃是烷烃,则形成烷基。
举例
例如,-CH3叫甲基,-CH2CH3叫乙基等。烷基的通式为为CnH2n+1,一般常用-R表示各类烷基。
强调
在学习时要注意,烃基不带电荷,不可单独存在。烃基的书写规范,不可缺少键线,否则,为错误。
板书
2.烷烃的同分异构现象。
讲述
在研究物质的分子组成和性质时,发现有不少物质的分子组成相同,但性质却有差异。例如,在研究丁烷(C4H10)的组成和性质时,就发现有另一种组成和相对分子质量与丁烷完全相同,但性质却有差异。为了区别起见,把其中的一种叫做正丁烷,另一种叫做异丁烷。
参考
教材表5-3。
问题
为什么这两种丁烷具有相同的组成和相对分子质量,但却具有不同的性质呢?
分析
经过科学实验证明,原来它们的结构是不同的。正丁烷分子里的碳原子形成直链,而异丁烷分子里的碳原子却带有支链。
板书
正丁烷 异丁烷
结构式 CH3-CH2-CH2-CH3 CH3-CH-CH3
CH3
讲述
像这种化合物具有相同的分子式,但是具有不同结构的现象,叫做同分异构现象。具有同分异构现象的化合物互称为同分异构体。
板书
同分异构体——分子式相同,结构不同。
讲述
在烷烃同系物的分子中,随着碳原子数目的增加,碳原子间的结合方式就越复杂,同分异构体的数目也就越多。
举例
含有4个碳原子的丁烷有两种同分异构体,含有5个碳原子的戊烷有3种同分异构体,而含有7个碳原子的庚烷有9种,而含有10个碳原子的癸烷多达75种。
解释
有机化合物中,碳和碳可以相互连接向空间多向伸展,形成同分异构体,这是有机物数目巨大的重要原因。
板书
3.烷烃的命名
讲述
烷烃的命名,常采用习惯命名法和系统命名法。
板书
(1)习惯命名法。
讲解
习惯命名法是根据分子里所含的碳原子的数目来命名的。碳原子数在10个以下的,依次用甲、乙、丙、丁、戊、己、庚、辛、壬、癸来命名。
举例
如甲烷CH4、辛烷C7H16。碳原子数在10个以上的用数字来命名,如C11H24叫十一烷。
板书
(2)系统命名法
讲解
对于直链烷烃,其命名方法和习惯命名法相同。
边讲边举例板书
对于带有支链的烷烃,其规则为:
第一,确定主碳链。选择分子里最长的碳链作为主链,并按主链上碳原子的数目称为“某烷”。
第二,给主碳链编号。当主链上有支链时,要对主链上的碳原子进行编号,以确定支链的位置。编号的方法是从离支链较近的一端开始,依次用阿拉伯数字1、2、3、…给主链上的每个碳原子编号。经编号确定了位置的支链(烷基)被作为取代基,将取代基的位置、名称写在某烷的前面,并用一条短线“-”将阿拉伯数字与文字隔开。
举例
例如:下列化合物按普通命名法称为异戊烷,而按系统命名法则被命名为2-甲基丁烷。
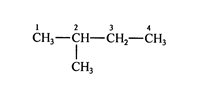
 
 
 
第三,确定支链(取代基)的位置、数目和名称。当烃分子里有几个相同的取代基时,要把定位数字用逗号隔开,并把取代基数目合并起来用二、三、四……数字表示。
第四,命名。
举例
例如:下列化合物按系统命名法则被命名为2,2-二甲基戊烷。
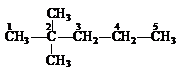
 
 
 
强调
若烃分子里有几个不相同的取代基时,命名时应把简单的写在前面,复杂的写在后面。
举例
例如
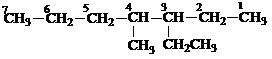
4-甲基-3-乙基庚烷
注意
在学习烷烃的系统命名法时应注意两点:一是序号用阿拉伯数字,个数用汉字;二是序数之间用“,”,基序之间用“-”。
投影
课堂练习
1.下图是一种烃的结构式,命名该化合物时,主链上的碳原子数是( )。
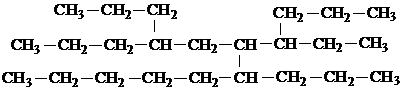
A. 9 B. 11 C. 12 D. 13
2. 烃分子可以看作由以下基团组合而成,如某烷烃分子中同时存在这四种基团,则该烷烃最少含有的碳原子数应是( )。
![]()
A. 6 B. 7 C. 8 D. 10
过渡
在具有链状分子结构的烃里,除了饱和链烃外,还有一些烃,分子里的碳原子所结合的氢原子数较含有相同数目碳原子的饱和链烃分子中的氢原子数少,这类链烃叫做不饱和链烃。“不饱和”意味着它能够再与其他原子结合生成饱和的化合物。乙烯(C2H4)就是一种不饱和链烃。
板书
二、乙烯、烯烃
(一)乙烯
1.乙烯的组成与结构。
投影
分析乙烯结构。
![]()
板书
![]()
(1)结构:分子式为C2H4,电子式为 ,结构式为 ,空间构型为平面构型。
板书
2. 乙烯的性质。
讲解
乙烯是无色稍有气味的气体,密度与空气接近,难溶于水。
乙烯的分子结构特点是含有碳碳双键,双键中有一个键稳定,另一个键很不稳定,在一定条件下,易于断开,所以,与只含有碳碳单键的烷烃相比,乙烯的化学性质比甲烷活泼,较易发生化学反应。
引导
与甲烷一样,乙烯能在空气里燃烧。但火焰比甲烷明亮并伴有黑烟生成,燃烧产物都是二氧化碳和水。
板书
燃烧
(1)氧化反应。
CH2=CH2(气)+ 3O2(气) CO2(气)+ 2H2O(液)
讲解
把乙烯通入盛有酸性高锰酸钾溶液的试管里,可以看到,溶液的紫色很快褪去,表明乙烯能被高锰酸钾氧化。这个反应说明乙烯的化学性质比甲烷活泼。用这一反应可以区别甲烷和乙烯。
投影
课堂练习
甲烷中混有乙烯,欲除乙烯得到纯净的甲烷,可依次将其通过下列哪组试剂的洗气瓶( )。
A. 澄清石灰水,浓H2SO4 B. 溴水,浓H2SO4
C. 酸性高锰酸钾溶液,浓H2SO4 D. 浓H2SO4,酸性高锰酸钾溶液
讲解
把乙烯通入盛有溴水的试管里,不需要光照、催化剂或加热,溴水的红棕色很快消失。这是由于乙烯跟溴水中的溴起反应,生成无色的1,2-二溴乙烷。
板书
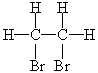
![]()
![]()
+ Br2
1,2-二溴乙烷
讲解
在这个反应中,乙烯分子双键中的一个键断裂,两个溴原子分别加在两个原来以双键相连的不饱和碳原子上,生成了1,2-二溴乙烷。这种在有机物分子中,双键(或三键)两端的碳原子与其他原子或基团直接结合生成新的化合物的反应,叫做加成反应。
板书
(2)加成反应。
强调
双键(或三键)两端的碳原子与其他原子或基团直接结合生成新的化合物的反应,叫做加成反应。
由于这一反应现象明显,常被用来鉴别乙烯等不饱和链烃。
讲述
除溴水外,在适宜的条件下,乙烯还能和许多物质(如氢气、氯气、卤化氢、水)发生加成反应。
引导
乙烯分子不仅能和许多试剂发生加成反应,而且在适当的条件下,其自身也能相互加成生成大分子的聚合物。
板书
![]()
催化剂
(3)聚合反应。![]()
n CH2=CH2
聚乙烯
概念
这种在一定条件下,由相对分子质量小的化合物分子互相结合成相对分子质量大的高分子化合物的反应,叫做聚合反应。
讲述
乙烯聚合反应的产物叫聚乙烯,是一种相对分子质量很大(几万到几十万)的化合物。聚乙烯无毒、无味、质轻、化学稳定性好,应用很广泛。可用于制造农用塑料薄膜、自来水管、食品包装袋、水壶、茶杯、贮油桶等。聚乙烯是目前塑料中产量最大的一个品种。
引导
参考课本找出乙烯的用途。
板书
3. 乙烯的用途。
工业原料、催熟剂。
过渡
除乙烯外,还有与乙烯在组成上相差一个或多个CH2基团的一系列同系物。
举例
CH2=CH—CH3 丙烯
CH2=CH—CH2—CH3 1-丁烯
CH2=CH—CH2—CH2—CH3 1-戊烯
板书
(二)烯烃
它们的分子结构中都含有一个双键,比含有相同碳原子数的烷烃要少两个氢原子,所以烯烃的通式为CnH2n(n≥2)。
讲述
烯烃的物理性质一般也随着碳原子数目的增加而有规律地变化。烯烃的化学性质与乙烯相似,能发生加成反应、聚合反应和氧化反应;能使溴水、高锰酸钾酸性溶液褪色。
过渡
学习过甲烷和烷烃、乙烯和烯烃后我们再来认识另外一种典型的烃。
板书
三、乙炔、炔烃
(一)乙炔
1.乙炔分子的组成与结构。
投影
分析乙炔结构。
板书
![]()
分子式为C2H2,电子式为 ,结构式为H―C≡C―H,空间结构为直线形构型。
讲述
乙炔俗名电石气。用电石制得的乙炔由于混有少量的磷化氢、硫化氢等气体而具有难闻的臭味。纯净的乙炔是无色、无味的气体。在标准状况下,乙炔的密度是1.16 g/L,比空气稍轻。乙炔不易溶于水,易溶于有机溶剂。压强为1 215.9 kPa时,1体积丙酮可溶解300体积乙炔。乙炔在高温下易发生爆炸,但溶于丙酮后却很稳定。所以通常将乙炔溶于丙酮中进行运输、贮存。
板书
2. 乙炔的性质。
讲解
乙炔的分子结构特点是含有碳碳三键。三键中有一个稳定,另两个键不稳定,易于断裂,具有较大的活动性,所以乙炔的化学反应主要发生在三键上,碳碳三键是乙炔的官能团。
板书
(1)加成反应。
演示
演示教材实验5-1,引导学生观察溶液颜色的变化。和乙烯一样,乙炔能使溴水褪色,生成物为溴代烷。乙炔与溴的反应是分步进行的。
投影
 
1,1,2,2-四溴乙烷
1,2-二溴乙烯
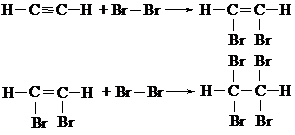
讲述
乙炔和氯化氢加成可生成氯乙烯。氯乙烯是生产聚氯乙烯塑料的原料。
催化剂
板书![]()
CH≡CH + HCl CH2=CHCl
氯乙烯
讲解
乙炔燃烧时产生大量的热(反应热2 599.1 kJ/mol)。乙炔在氧气中燃烧,产生的氧炔焰温度可达到3 000 ℃左右,因此可用来切割或焊接金属。
展示
图片。
板书
燃烧
(2)氧化反应。
2C2H2(气)+ 5O2(气) 4CO2(气)+ 2H2O(液)
说明
乙炔可以使高锰酸钾溶液褪色。
乙炔是重要的化工原料,以乙炔为原料通过一系列反应制得的聚氯乙烯是一种通用塑料。其原料来源丰富、低廉,耐腐蚀,电绝缘性好,容易加工成各种软、硬透明制品,如雨衣、凉鞋等;并具有较好的机械性能,广泛用于化工业、电器材料以及农业生产上。由聚氯乙烯树脂加工成型的薄膜,目前在农村多用于种植业。南方农村采用的水稻膜育秧,水稻发芽率高、苗壮、苗齐,深受群众欢迎。北方农村广泛采用的塑料大棚,一年四季都能生产蔬菜。但是,因聚氯乙烯有毒,易造成土壤环境污染,除切忌作食品袋外,将来作为农用薄膜也要限制使用。目前,正在研究以淀粉为原料制造农用薄膜。
板书
3. 乙炔的用途。
化工原料。
(二)炔烃
链烃分子里含有碳碳三键的不饱和烃叫炔烃。
讲述
乙炔、丙炔、丁炔、戊炔等一系列同系物构成炔烃。炔烃分子中三键的存在,使其在组成上较相应的烯烃又少了两个氢原子,所以炔烃的通式为CnH2n-2(n≥2)。炔烃的命名与烯烃相似。与乙炔一样,炔烃能发生氧化、加成等一系列化学反应。
强调
在学习各类烃时,要重视烃的结构与性质之间的关系。性质是由结构决定的。在学习各类烃的分子结构时,应重点把握住碳碳键的键型不同,物质的性质也不同。
小结
烷烃、烯烃、炔烃的结构和性质,以及它们各自的代表物质甲烷、乙烯、乙炔的性质和用途。
作业
课后思考与练习。
 
【板书设计】
第二节 烃
仅含有碳和氢两种元素的有机化合物叫烃。

CnH2n+2(n≥1)
 
CnH2n(n≥2)
CnH2n-2(n≥2)
CnH2n(n≥3)
CnH2n-6(n≥6)
 
 
 
 
 
一、甲烷 烷烃
(一)甲烷
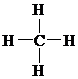
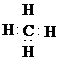
1. 甲烷分子的组成与结构。
甲烷的结构:分子式为CH4,电子式为 ,结构式为 ,空间结构为正四面体。
2. 甲烷的性质。
燃烧
(1)氧化反应。
CH4 + 2O2 CO2↑ + 2H2O
光
(2)取代反应——有机物分子里的某些原子或基团被其他原子或基团所替代的反应叫做取代反应。![]()
CH4 + Cl2 CH3Cl + HCl
光
一氯甲烷光
CH3Cl + Cl2 CH2Cl2 + HCl
光
CH2Cl2 + Cl2 CHCl3 + HCl
![]()
CHCl3 + Cl2 CCl4 + HCl
3. 甲烷的用途——燃料、工业原料。
(二)烷烃
1.烷烃的概念。
只有碳碳单键和碳氢键的链烃叫做饱和链烃,也称烷烃。
把结构相似,在分子组成上相差一个或若干个CH2基团,并具有同一通式的一系列化合物互称为同系物。
烃分子失去一个氢原子后所剩余的基团叫做烃基。
2.烷烃的同分异构现象。
正丁烷 异丁烷
结构式 CH3-CH2-CH2-CH3 CH3-CH-CH3
CH3
同分异构体——分子式相同,结构不同。
 
3.烷烃的命名
(1)习惯命名法
(2)系统命名法
对于带有支链的烷烃,其命名规则为:
第一,确定主碳链,定母体。选择分子里最长的碳链作为主链,并按主链上碳原子的数目称为“某烷”。
第二,找准起点,给主碳链编号。以离支链较近的一端为起点开始编号。
第三,确定支链(取代基)的位置、数目和名称。
第四,命名。
注意:在学习烷烃的系统命名法时应注意两点:一是序号用阿拉伯数字,个数用汉字;二是序数之间用“,”,基序之间用“-”。
二、乙烯、烯烃
(一)乙烯
![]()
1. 乙烯的组成与结构
![]()
(1)结构:分子式为C2H4,电子式为 ,结构式为 ,空间构型为平面构型。
2. 乙烯的性质
燃烧
(1)氧化反应
CH2=CH2(气)+ 3O2(气) CO2(气)+ 2H2O(液)
(2)加成反应
![]()
CH2=CH2 + Br2 CH2BrCH2Br
催化剂
乙烯可使溴水腿色,这一反应也可用溴水区别甲烷和乙烯。![]()
![]()
(3)聚合反应:nCH2=CH2
3. 乙烯的用途
工业原料、催熟剂。
(二)烯烃
通式为CnH2n(n≥2)。
三、乙炔、炔烃
(一)乙炔
1. 乙炔分子的组成与结构
![]()
分子式为C2H2,电子式为 ,结构式为H―C≡C―H,空间结构为直线形构型。
2. 乙炔的性质
(1)加成反应
催化剂
CH≡CH + HCl CH2=CHCl
氯乙烯
燃烧
(2)氧化反应
2C2H2(气)+ 5O2(气) 4CO2(气)+ 2H2O(液)
乙炔可以使高锰酸钾溶液褪色。
3. 乙炔的用途
乙炔可以用作化工原料。
(二)炔烃
链烃分子里含有碳碳三键的不饱和烃叫炔烃,通式为CnH2n-2(n≥2)。
 
 
 
 
 
180
 

 负责人:黄剑鹏
负责人:黄剑鹏